Bildnachweis: is_AdobeStock.
Die börsennotierte Clinuvel-Gruppe mit Sitz in Melbourne, Australien (Market Cap: rund 700 Mio. AUD, [ca. 430 Mio. EUR]), ist ein weltweit tätiges biopharmazeutisches Unternehmen, das über herausragende Expertise im Bereich der Melanocortin-Produkte verfügt. 55 Mio. EUR erwarteter Umsatz 2024 und eine EBIT-Marge von fast 50 % – und das bei einer Cash-Position von über 120 Mio. EUR – machen die Aktie (ISIN AU000000CUV3) interessant. Aus der Historie heraus hat das Unternehmen zudem eine große Aktionärsbasis in Deutschland. Rund 25 Jahre war es rund um Clinuvel, die in den Anfängen noch unter „EpiTan“ firmierten, ruhig geblieben. Erst mit dem Einstieg des heutigen Vorstandschefs Philippe Wolgen kam 2005 die Wende und es entwickelte sich eine klassische Turnaround Story. Anlass genug, um mit CEO Dr. Philippe Wolgen über Alleinstellungsmerkmale, unkonventionelle Denkmuster und Zukunftspotenziale zu sprechen.
GoingPublic: Viele biopharmazeutische Unternehmen, die Pionierarbeit in einem spezifischen Bereich geleistet haben, genießen hohe Bekanntheit wie zum Beispiel Biogen, Eli Lilly, CureVac oder Incyte. Warum bleibt Clinuvel als Pionier der Photomedizin in vielen Fällen unterhalb des Radars?
Dr. Philippe Wolgen: Aufgrund unserer Historie hatten wir uns als Spezialpharmaunternehmen ausschließlich auf seltene Krankheiten – sogenannte orphan diseases – fokussiert, die durch Sonnenlicht verursacht werden. Dazu zählt beispielsweise die Erythropoetische Protoporphyrie (EPP), welche im Volksmund auch nicht ganz zutreffend als „Schattenspringer-Krankheit“ bezeichnet wird. Aufgrund eines Gendefekts reichert sich phototoxisches Protoporphyrin in den Erythrozyten und im Blutplasma an, nimmt Lichtenergie auf, überträgt sie ans umgebende Gewebe und löst dort Verbrennungen aus. Eine sehr schmerzhafte Krankheit, die ein normales Leben mit alltäglicher Lichtexposition kaum möglich macht. Dank unseres Reiskorn-großen Implantats SCENESSE®, das an der Hüfte eingesetzt wird und das dort kontinuierlich den Wirkstoff Afamelanotid abgibt, können Betroffene sich wieder unbeschwert in der Sonne aufhalten. Da SCENESSE® gleichzeitig das einzige verschreibungspflichtige Medikament ist, das bei EPP für den kommerziellen Vertrieb in Europa, den USA, Kanada, Israel und Australien zugelassen ist, genießen wir ein Alleinstellungsmerkmal – ich kann insofern relativieren, dass wir unter EPP-Betroffenen eine Bekanntheit von nahezu 100 Prozent haben.

Sie haben mit Ihrer Fragestellung eigentlich schon die Antwort gegeben. Trader haben nur das Pricing im Auge, Investoren interessieren sich für Value. Wir hatten damals gerade erst angefangen Werte zu bilden, aber der Börsenkurs eilte uns voraus und erreichte irrwitzige Ausmaße mit einem dreistelligen KGV. Am Telefon und in E-Mails zeigten sich Aktionäre überglücklich und feierten uns wie Rockstars. Auch Analysten waren voll des Lobes für unsere Arbeit. Ich machte aber bereits damals deutlich, dass dieser Aktienpreis nichts, aber auch gar nichts mit uns als Unternehmen zu tun hatte, sondern eine unrealistische Übertreibung darstellte. Das ist ja das Verrückte am Aktienmarkt, dass die Börse Hoffnungen und Visionen handelt. In dem Moment wo sie eintreten, fällt der Preis – die Fantasie ist raus. Eine Form von elektronischem Casino, bei dem man mitspielen kann oder auch nicht. Wir fühlen uns jetzt, da der Preis zwar nur mehr ein Drittel beträgt, aber der intrinsische Wert sich verdreifacht hat, bedeutend wohler, da mit diesem Wert das organische, zukünftige Wachstum finanziert werden kann. Wenn wir unsere zukünftigen Potenziale – und davon gibt es jede Menge – schöpfen, wird der Börsenkurs automatisch weiter nach oben gehen. Unser Weg ist ein Marathon, kein Sprint.
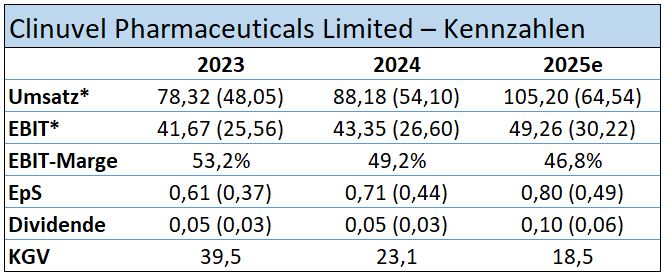
Dass Sie auf dem richtigen Weg sind, belegen auch die jüngsten Geschäftszahlen. Acht Wachstumsjahre in Folge, zweistellige Zuwachsraten bei Umsatz und Gewinn in den letzten Jahren, Dividendenzahlungen seit dem Geschäftsjahr 2018, hoher Cashbestand von 200 Mio. AUD (122,7 Mio. EUR) und ein bemerkenswert niedriger Verschuldungsgrad von 14 Prozent – alles nicht unbedingt typisch für den kapitalintensiven Biopharma-Sektor. Was macht Clinuvel anders?
Eigentlich alles – das beginnt schon mit der strikten Fokussierung auf ein Produkt. Die meisten Pharmaunternehmen diversifizieren am Anfang und forschen in alle Richtungen und nur eins dieser Gebiete funktioniert. Wir sind den anderen Weg gegangen und haben ein Unternehmen um SCENESSE® gebaut. Zudem haben wir alles in der eigenen Hand behalten: vollständige Kontrolle über das Pricing, kein Outsourcing, keine externe Distribution. Wir beliefern und arbeiten also direkt mit den einzelnen medizinischen Centern zusammen, von denen im Schnitt jedes Jahr 20 bis 25 neue hinzukommen. Das war am Anfang zugegebenermaßen ein logistischer Alptraum, weil man in Konkurrenz zu Giganten wie Pfizer oder Roche tritt. Aber einmal installiert und implementiert ist es viel kosteneffizienter direkt zu beliefern, vorausgesetzt, man hat ein gutes Team. Und Clinuvel hat ein sehr gutes Team. Mein Management-Team besteht seit 20 Jahren, da gibt es so gut wie keine Fluktuation. Ein Ansatz, der sich bewährt hat, zumal so auch das Wissen im Unternehmen bleibt. Zudem haben wir einen etwas anderen wirtschaftlichen Ansatz. Wir packen – bildlich gesprochen – das Geld auf die Bank und versuchen nicht mehr auszugeben als das was reinkommt. Dieser typisch kaufmännische Ansatz, der komplett unüblich für die Biopharmaziebranche ist, gibt uns ein mächtiges Instrument an die Hand, denn man agiert aus einer Position der Stärke heraus und ist weniger leicht angreifbar.
Gleichwohl muss sich Clinuvel der Kritik aussetzen, dass man als „Einprodukt-Unternehmen“ wirtschaftlich komplett von SCENESSE® abhängig ist. Birgt das nicht große Risiken, gerade wenn der Patentschutz ausläuft?
Dies ist eine Fehleinschätzung, der man leicht erliegen kann, wenn man sich nicht eingehend mit der biopharmazeutischen Materie beschäftigt. Man muss SCENESSE® als Plattformtechnologie verstehen, die für drei und mehr Indikationen angewendet werden kann. Bei einer Tech-Company, die Mikrochips herstellt, würde man auch nicht sagen: „Ihr produziert nur einen Mikrochip, habt also nur ein Produkt!“ Entscheidend ist vielmehr, in welchen Bereichen der Chip zum Einsatz kommt. Im Zeitraum zwischen 2026 bis 2033 wird die Patentexklusivität für die Behandlung von EPP-Patienten mit Afamelanotid auslaufen. Zu diesem Zeitpunkt haben wir längst die flächendeckende Expansion in den USA abgeschlossen. Mit ca. 120 Medizincentern, die sich in allen Bundesstaaten der USA befinden, haben wir dann individuelle Verträge, Leistungskataloge und Abrechnungsmodelle, ebenso wie mit Versicherern und Kliniken. Das ist darum so wichtig, weil es in den USA kein zentral geführtes Krankenkassenmodell wie in Deutschland gibt – jeder Bundesstaat muss also separat bearbeitet und verwaltet werden. Das wird natürlich auch für zukünftige Konkurrenten eine nicht unerhebliche Hürde sein. Noch wichtiger ist aber das sukzessiv aufgebaute Netzwerk. Insofern sollte man den bisherigen Erfolg als Testlauf verstehen – die eigentliche Story fängt gerade erst an.
Das müssen Sie uns näher erläutern!
Wir sehen EPP als Vorstufe zum eigentlich großen Markt, nämlich der Weißfleckenkrankheit (Vitiligo), die eine ganz andere Dimension aufweist. Ungefähr 0,5 bis 1 Prozent der weltweiten Bevölkerung leidet unter dieser Pigmentstörung, die sich durch weiße Flecken auf der Haut äußert. Zum Vergleich: die weltweite Prävalenz bei EPP liegt gerade einmal bei 1 zu 150.000. SCENESSE® in Anwendung bei Vitiligo – das ist das eigentlich Ziel, da muss Clinuvel hin und darauf haben wir den Markt und die rund 8.000 Zentren in den USA eingestimmt und in jahrelanger Kleinarbeit vorbereitet. Wir wissen, dass wir mit SCENESSE® nicht nur ein exzellentes Produkt haben, sondern, dass es auch wirkt! Innerhalb von nur einer Woche sieht man, ob die Haut reagiert hat oder nicht und im Idealfall haben sich die Flecken zurückgebildet. Tatsächlich habe ich kein anderes Produkt auf der Welt gesehen, bei dem man so gut sehen kann, ob es funktioniert oder nicht: die kritische Frage ist also nicht die Wirkung, sondern die Distribution und die Überzeugungsarbeit, die bei Ärzten geleistet werden muss, damit sie das Mittel bei Vitiligo verschreiben. Und natürlich die Erstattungsfähigkeit durch die dezentralen Krankenkassen – alles Faktoren, bei denen wir mit EPP in Vorleistung gegangen sind.
Sie erwähnten drei und mehr Indikationen für SCENESSE®. Welche weiteren sind das konkret und wie ist da der aktuelle Stand?
Neben EPP und Vitiligo (Phase-III-Studie gestartet) wären Anwendungen bei den seltenen Erbkrankheiten Xeroderma pigmentosum (XP) und Variegate Porphyrie (VP) zu nennen, wobei sich die beiden letztgenannten jeweils in „Phase-IIa-Tests“ befinden. Zudem wird aktuell eine flüssige Formulierung des Wirkstoffs Afamelanotid für die Akutversorgung von Schlaganfallpatienten unter dem Namen PRÉNUMBRA® Instant (geschätzte Zulassung 2028) getestet. Diese flüssige Formulierung erscheint auch bei der Behandlung von Patienten mit Parkinson vielversprechend (einarmige klinische Phase-IIa-Studie im Juni 2024 gestartet). Darüberhinaus schlagen wir mit NEURACTHEL® Instant, einem ACTH-Generikum für rheumatische und Autoimmun-Erkrankungen, einen ganz neuen Weg ein – mit der Zulassung rechnen wir im Jahr 2026, also auch relativ zeitnah.
Mit dem Launch der PhotoCosmetics-Linie Cyacêlle im März 2023 hat Clinuvel sein Produktportfolio ebenfalls diversifiziert und den OTC-Markt betreten. Liegt das nicht sehr weit weg von der eigentlichen Kernkompetenz?
Ganz im Gegenteil, dann damit schließt sich der Kreis. Die Geschichte von Clinuvel beginnt 1987, als vier Forscher ein Hormon entdeckten, welches die Haut ohne Sonneneinwirkung braun machen konnte. Das Medienecho war überwältigend – Zeitungen, Radiosendungen und Fernsehberichte überschlugen sich mit Meldungen zur sogenannten „Barbie-Droge aus Australien“. Allerdings gab es einen Haken. Es gab keine medizinische Anwendung, denn keine Behörde hätte jemals das Einspritzen dieses Hormons zum Zweck der Selbstbräunung erlaubt, schließlich gab es keine Langzeitstudien und auch kein Wissen über mögliche Nebenwirkungen. Von 1990 bis 2005 haben alle großen Kosmetikfirmen wie beispielsweise L’Oréal, Coty, Estée Lauder, Johnson & Johnson oder P&G Teile des Hormons in ihre Cremes gegeben und sie als Selbstbräunungscremes auf den Markt gebracht. Der Erfolg blieb aber aus, weil Kosmetikfirmen ihre Produkte viel zu schnell zur Marktreife bringen müssen. Das liegt in der Natur dieser Branche. Tests hingegen müssen über einen Zeitraum von 10 bis 15 Jahren erfolgen, unter Beteiligung von Probanden, also ein ganz anderes Geschäftsmodell. Und hier kommen wir wieder ins Spiel. Wir haben diese Daten, wir kennen das Produkt und wir sehen, dass unser Produkt auch unter medizinischen Aspekten wirkt und funktioniert. Insofern ist die OTC-Lancierung, die übrigens um weitere Linien erweitert wird, die logische Kombination von hochwertiger Luxus-Kosmetik mit medizinisch validen Daten und Tests.
Herr Dr. Wolgen, vielen Dank für die spannenden Ausführungen!
Das Interview für GoingPublic führte Marcantonio Moschettini.
Zum Interviewpartner

Autor/Autorin

Marc Moschettini
Marc Moschettini ist Mitglied des GoingPublic-Autoren-Teams. Er studierte BWL an der LMU München/ ESC Lyon und ist seit über 15 Jahren als freier Wirtschafts- und Finanzjournalist tätig. In den Bereichen Aktien, Fonds und Derivate publiziert er im deutschsprachigen Raum u.a. für Fachmagazine, Onlineplattformen und Newsletter.






